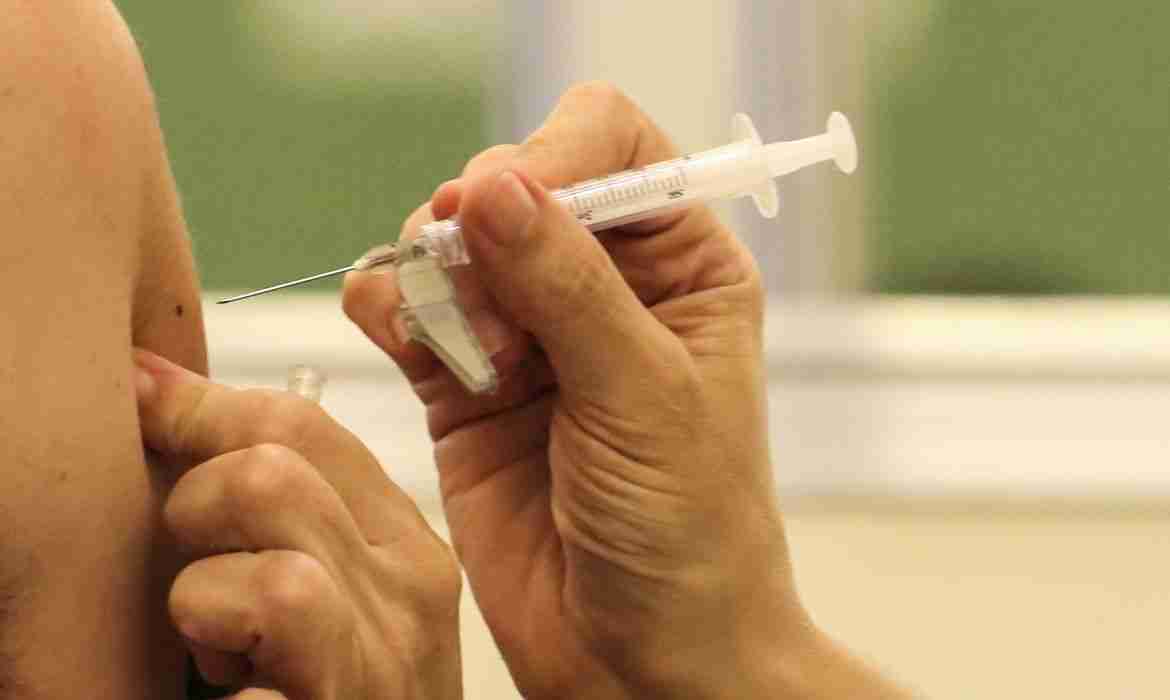
A Anvisa (Agência Nacional de Vigilância Sanitária) autorizou nesta quarta-feira (7) o início da vacinação de voluntários do estudo clínico da Butanvac, a vacina contra o novo coronavírus que está em desenvolvimento pelo Instituto Butantan.
+Força Aérea dos EUA revela nova imagem do B-21 Raider
+ Motorola Moto G9 Play começa a receber atualização para o Android 11
+ Fórum da Internet no Brasil está com inscrições abertas
+ Yandex vai implantar serviço de entrega com robôs em universidades dos EUA
+ BTS divulga novo filtro no Instagram
A pesquisa clínica de fase 1 e 2 da Butanvac está dividida em três etapas (A, B e C). Neste momento, está autorizada a etapa A do estudo, que vai envolver 400 voluntários. Ao todo, as fases clínicas 1 e 2 têm previsão de seis mil voluntários com 18 anos ou mais.
A vacina será aplicada com duas doses, em um intervalo de 28 dias entre a primeira e a segunda dose. O estudo deve ser realizado no Hospital das Clínicas da Faculdade de Medicina da Universidade de São Paulo e no Hospital das Clínicas da Faculdade de Medicina de Ribeirão Preto.